Cтиральные порошки, cредства для мытья посуды, мыло и многие другие моющие средства — почему они так хороши в борьбе с загрязнениями? Если прочитать их состав, то можно найти загадочную аббревиатуру ПАВ. Что же это такое?
МОЛЕКУЛЫ ЧИСТОТЫ
Поверхностно-активное вещество — именно так расшифровывается аббревиатура ПАВ — это главный компонент моющих средств: собственно, он обеспечивает очищающую функцию. Молекула ПАВ состоит из двух частей — длинной углеродной цепочки, которая вступает в контакт с жиром, и фрагмента, который притягивает молекулы воды. Именно благодаря этому свойству поверхностно-активные вещества позволяют смывать жирный налёт и загрязнения.

Допустим, вы ели рыбу. На поверхности рук рыбий жир, который водой ну никак не хочет отмываться. Мы наносим на руки мыло, которое содержит ПАВ — стеарат натрия.
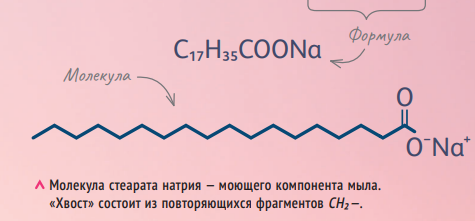
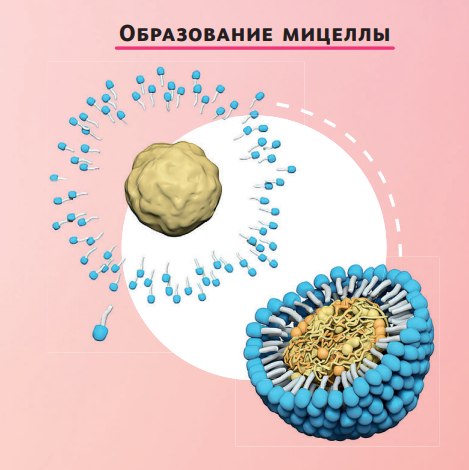
Эта молекула — хороший пример ПАВ. У неё есть длинный неполярный «хвост» и полярная гидрофильная «голова». Слово «гидрофильный» означает, что молекула или её часть хорошо связываются с водой. ПАВ погружаются «хвостами» в капли жира, а торчащие наружу гидрофильные «головы» связываются с молекулами воды. Образуются микроскопические частицы, называющиеся мицеллы, а уж они, в свою очередь, легко смываются водой. Помните, что в косметической индустрии для снятия макияжа часто используют мицеллярный раствор, который советуют обильно смывать водой после использования? Основу такого средства составляют мицеллы жирных кислот, окружённые жидкой средой, — раствор, попадая на кожу, «притягивает» грязь и жир.
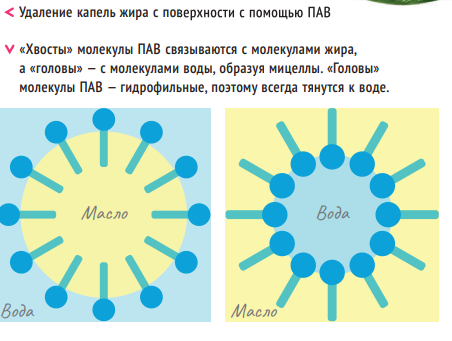
ВОДОЙ МАСЛО НЕ ОТМОЕШЬ
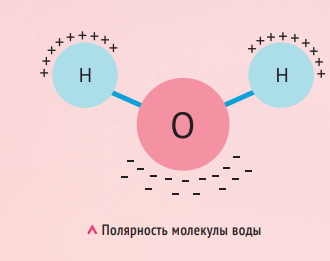
Формула воды — H₂O (два атома водорода и один атом кислорода). Электроотрицательность кислорода выше, чем у водорода, а значит, кислород будет перетягивать отрицательно заряженные электроны на себя — тут, как и в жизни, противоположности притягиваются. В итоге на кислороде возникнет избыточный отрицательный заряд, а на водороде — избыточный положительный. Такие молекулы считаются полярными и могут электрически притягиваться к другим таким же молекулам (например, ацетона). Вода является полярным растворителем.
Но почему в воде не растворяются масло и некоторые другие вещества? Если налить в стакан с водой бензин, то они не смешаются!
Бензин — это смесь углеводородов, один из самых важных в его составе — гептан. Его молекула состоит из углерода и водорода. Значения электро отрицательности углерода и водорода близки, поэтому в молекуле атомы сильно не перетягивают электроны друг у друга, и никаких избыточных зарядов не образуется. В случае гептана молекула неполярна.
А полярные и неполярные вещества не растворяются друг в друге, и когда мы смешиваем «полярную» воду с «неполярным» бензином, то никакого смешения не происходит! Поэтому, к сожалению, без мыла масло водой никак не смоешь.

КОГДА ВЕЩЕСТВАМ ТЕСНО
В 1917 году химик И Л ( ) обнаружил, что некоторые вещества очень активно накапливаются на различных пограничных поверхностях (например, на границе тех же воды и масла).
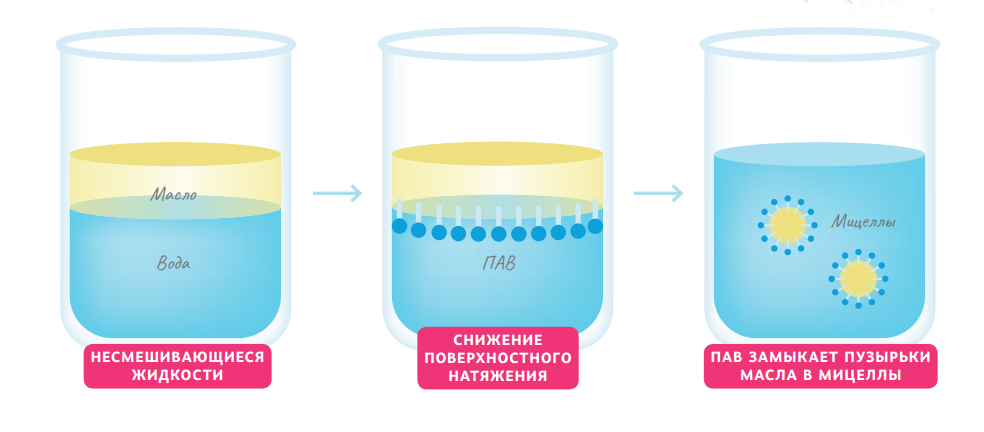
Причина поверхностного натяжения в том, что молекулы, находящиеся на поверхности, не испытывают тех же сил притяжения от «своих», что испытывают молекулы в объёме. Это создаёт внутреннее давление и вынуждает максимально сокращать поверхность жидкости. Именно поэтому маслу и воде в стакане выгоднее разделиться на два слоя, а не, скажем, образовать много маленьких пузырьков.
В результате на границе «вода— масло» оказывается слой молекул, силы притяжения которых не скомпенсированы. А ПАВ, добавленное в смесь масла и воды, снижает такое поверхностное натяжение.
При контакте ПАВ с поверхностью жидкости или твёрдого тела происходит процесс адсорбции — молекулы поверхностно-активного вещества накап ливаются на так называемой границе. В результате свойства загрязнений, покрытых адсорбционными слоями, резко изменяются: гидрофобные поверхности становятся более гидрофильными и начинаются лучше смачиваться водой.
В начале процесса адсорбции ПАВ растворяются в одной из пограничных фаз. Чем больше мы добавляем поверхностноактивных веществ, тем сильнее меняются свойства растворяемых. Формируется раствор, в котором ПАВ принимает вид уже знакомых нам мицелл.
До появления бытовой химии посуду часто мыли с использованием золы. Зола содержит смесь карбоната калия и карбоната натрия. Эти соединения являются солями очень сильной щёлочи (гидроксида калия) и очень слабой угольной кислоты. В результате щелочная составляющая побеждает, и при растворении золы (карбоната калия или натрия) в воде образуется щёлочной раствор. Щёлочь тоже взаимодействует с поверхностным натяжением. Но, в отличие от ПАВ, которые его понижают, она относится к ПИАВ, поверхностно-инактивным веществам, и повышает поверхностное натяжение, разрушая тем самым молекулы жира.
ЗНАМЕНИТЫЕ МОЙДОДЫРЫ
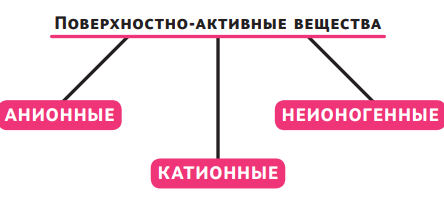
Поверхностно-активные вещества бывают анионными, катионными, неионогенными. Стеарат натрия, один из основных компонентов мыла, содержит ПАВ-компонент, полярная «голова» которого заряжена отрицательно. Такой фрагмент называется анионом, а ПАВ, устроенные похожим образом, называют анионными. Исторически это первые ПАВ, но у них есть свой недостаток: они активно взаимодействуют с катионами кальция и магния, которые содержатся в жёсткой воде. В результате моющее действие вещества пропадает.

У катионных ПАВ «голова» заряжена положительно. Они не очень хорошо отмывают, но обладают бактерицидными, консервирующими и антикоррозионными свойствами. Их используют существенно реже, зачастую в композиции с анионными или неионогенными веществами. В настоящее время большое значение имеет именно последний тип ПАВ.

Неионогенные ПАВ устроены сложнее, но принципиальная схема остаётся: «хвост», длинная углеродная цепочка и гидрофильная «голова». Они не взаимодействуют с ионами кальция и магния в жёсткой воде, и в этом их главное преимущество. Поэтому неионогенные ПАВ используют в стиральных порошках и других моющих средствах.
КАК ШАМПУНЬ ОЧИЩАЕТ ВОЛОСЫ
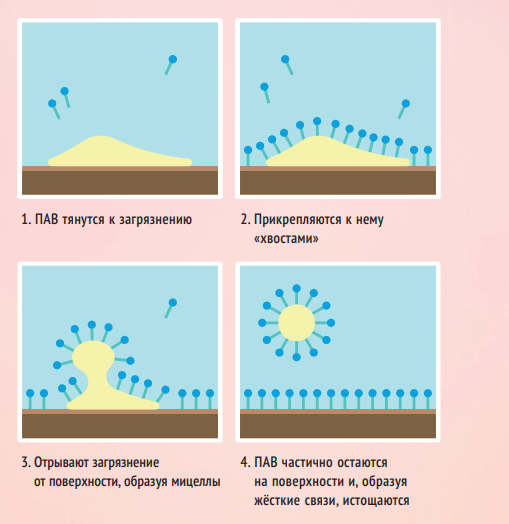
Эффект очищения в присутствии ПАВ достигается за счёт улучшения смачиваемости поверхности загрязнения и переведения его в форму раствора. Нерастворимый остаток разделяется на очень мелкие, покрытые слоем молекул ПАВ, частички (этот процесс называется диспергирование) удерживаются в растворе моющего средства (эмульгирование).
НЕ ВРЕДНЫ ЛИ ПАВ ДЛЯ ПРИРОДЫ И ЧЕЛОВЕКА?
Человечество каждый день выливает в стоки поверхностно-активные вещества. Несмотря на очистительные сооружения, часть из них попадает в почву и Мировой океан. Это, конечно, представляет определённый экологический риск. Наиболее опасными с точки зрения токсичности являются катионные вещества, менее вредны — анионные ПАВ, а неионогенные вещества — самые безопасные. На сегодняшний день большинство компаний-производителей используют анионные и неионогенные поверхностно-активные вещества, которые показывают более лёгкую биоразлагаемость.

Помимо поверхностно-активных веществ в моющих средствах ещё много компонентов. Для того, чтобы отмыть жир, достаточно и одного ПАВ, но важно не навредить рукам, которые часто взаимодействуют с бытовой химией. Поэтому в неё добавляют различные смягчающие компоненты — глицерин, масла, ароматизаторы и отдушки.
В состав стирального порошка, кроме анионных и неионогенных ПАВ, отдушек и ароматизаторов, входит множество других добавок: для поддержания кислотнощелочного баланса, умягчители воды (те, которые как раз борются с вредоносными катионами кальция и магния), энзимы (помогают удалить специфические пятна — белки, крахмал). Есть ещё много интересных и не самых очевидных применений. Например, ПАВ используются в нефтедобыче и строительстве; а ещё именно благодаря им существуют всеми любимые мыльные пузыри.






